Введение:
Введение:
Эффективная вакцинация против SARS-CoV-2 у пациентов, получающих лечение препаратами, разрушающими В-клетки, является сложной задачей. Информация о реакции на вакцинацию у этих пациентов является ценным инструментом для разработки эффективных схем вакцинации.
Методы:
В этом одноцентровом ретроспективном обсервационном исследовании мы сообщаем о гуморальном и клеточном ответе у 34 пациентов, получавших лечение антителами против CD20 по поводу иммунного заболевания почек.
Результаты:
После базовой иммунизации вакцинами SARS-CoV-2 у 92,0% развился клеточный, у 32,4% — гуморальный ответ. Гуморальный иммунитет коррелировал с количеством В-клеток и промежутком времени между лечением антителами против CD20 и вакцинацией. У всех пациентов с > 21/мкл В-клеток или > 197 дней после лечения наблюдался гуморальный ответ.
Выводы:
Адекватное время проведения вакцинации против SARS-CoV-2 после лечения антителами против CD20 и измерения уровня CD19 имеет решающее значение для формирования иммунитета. Пациентам со стабильным иммунным заболеванием следует рассмотреть возможность ожидания частичного восстановления В-клеток путем отсрочки регулярно назначаемого лечения анти-CD20.
Регистрация исследования:
Это исследование было ретроспективно зарегистрировано в Немецком реестре клинических испытаний (DRKS00027049) 29/10/2021.
Frederic Arnold, Daniela Huzly, Yakup Tanriver, Thomas Welte
BMC Infectious Diseases., 2022 September 14;22(1):73
DOI: 10.1186/s12879-022-07722-7
PMID: 36104663
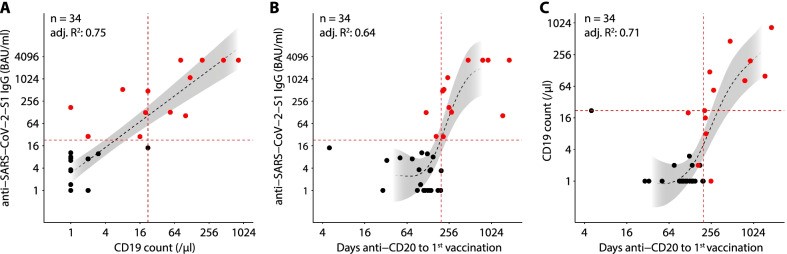
Fig. 1 SARS-CoV-2 Vaccination response correlates with…
Response to SARS-CoV-2 vaccines in patients receiving B-cell modulating antibodies for renal autoimmune disease
Background:
Effective SARS-CoV-2 vaccination in patients receiving treatment with B-cell depleting agents is challenging. Information on vaccination responses in these patients are a valuable tool to develop efficient vaccination regimens.
Methods:
In this single-center retrospective observational study, we report the humoral and cellular response in 34 patients receiving anti-CD20 antibody treatment for renal immune disease.
Results:
After base immunization with SARS-CoV-2-vaccines, 92.0% developed a cellular, 32.4% a humoral response. Humoral immunity correlated with B-cell counts and the timespan between anti-CD20 antibody treatment and vaccination. All patients with > 21/µl B-cells, or > 197 days after treatment showed humoral response.
Conclusions:
Adequate timing of SARS-CoV-2-vaccinations after anti-CD20 antibody treatment and CD19 measurements are crucial to generate immunity. Awaiting partial B-cell recovery by postponing regularly scheduled anti-CD20 treatment should be considered in patients with stable immune disease.
Trial registration:
This study has been retrospectively registered in the German Clinical Trials Register (DRKS00027049) on 29/10/2021.