МикроРНК представляют собой небольшие двухцепочечные РНК, которые отрицательно влияют на экспрессию генов, и играют ключевую роль как в развитии хондроцитов, так и в гомеостазе хряща с возрастом. Удаление всех микроРНК в хондроцитах приводит к дефектам роста скелета у мышей, в то время как удаление определённых микроРНК, например, miR-140, приводит к преждевременной деградации суставного хряща и повышенной восприимчивости к посттравматическому остеоартриту.
МикроРНК представляют собой небольшие двухцепочечные РНК, которые отрицательно влияют на экспрессию генов, и играют ключевую роль как в развитии хондроцитов, так и в гомеостазе хряща с возрастом. Удаление всех микроРНК в хондроцитах приводит к дефектам роста скелета у мышей, в то время как удаление определённых микроРНК, например, miR-140, приводит к преждевременной деградации суставного хряща и повышенной восприимчивости к посттравматическому остеоартриту.
Исследования, сравнивающие экспрессию микроРНК в нормальном суставном хряще человека и остеоартритном хряще, показывают дифференциальную экспрессию, но разные группы образцов затрудняют интерпретацию. МикроРНК были предложены как циркулирующие биомаркеры остеоартрита, но опять же, это различается для разных групп пациентов.
Было показано, что многие микро-РНК играют роль в фенотипе хондроцитов через сигнальные пути, апоптоз, аутофагию и старение. Было показано, что модуляция микроРНК в суставе снижает остеоартрит на животных моделях, и перевод этого на человека в качестве новой терапевтической стратегии будет ключевым.
Tracy E. Swingler, Lingzi Niu, Perry Smith, Paige Paddy, Linh Le, Matthew J. Barter, David A. Young, Ian M. Clark
Clinical and Experimental Rheumatology, Sep-Oct 2019, Volume 37 Suppl 120(5), pp 41-47
PMID: 31621575

The function of microRNAs in cartilage and osteoarthritis
MicroRNAs are small double-stranded RNAs, which negatively regulate gene expression and have been shown to have key roles in both chondrocyte development and cartilage homeostasis with age. Deletion of all microRNAs in chondrocytes leads to skeletal growth defects in mice, whilst deletion of specific microRNAs, e.g. miR-140, leads to premature articular cartilage degradation and increased susceptibility to posttraumatic osteoarthritis.
Studies comparing microRNA expression in normal human articular cartilage compared to osteoarthritic cartilage show differential expression, but varying sample groups make interpretation difficult. MicroRNAs have been proposed as circulating biomarkers of osteoarthritis, but again, this differs amongst patient cohorts.
Many micro-RNAs have been shown to have roles in chondrocyte phenotype via signalling pathways, apoptosis, autophagy and senescence. Modulating microRNAs in the joint has been shown to reduce osteoarthritis in animal models and translating this to man as a novel therapeutic strategy will be key.

Fig. 1. Biogenesis of microRNAs. MicroRNAs are transcribed as primary transcripts (pri-microRNAs) and processed by Drosha/DGCR8 to hairpin precursors (pre-microRNAs). These are exported to the cytoplasm and further processed by Dicer into the mature double-stranded microRNA. The duplex is unwound and one strand (guide) incorporated into RISC whilst the other strand (passenger) is degraded. The microRNA-RISC complex acts either to degrade its mRNA target where homology is high, or to inhibit translation, leading to mRNA degradation, where homology is lower.
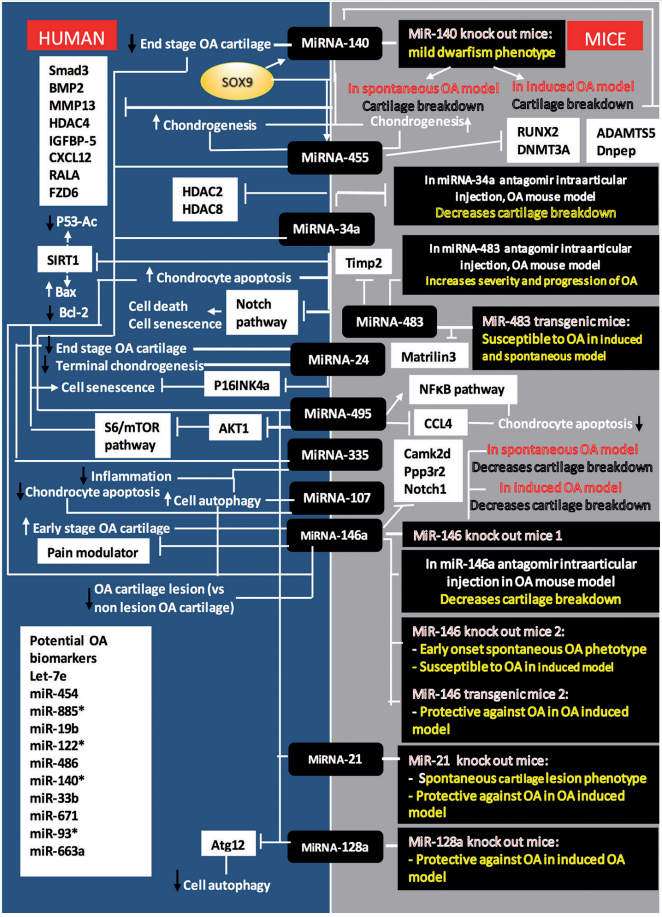
В остеоартритном хряще ряд микроРНК несёт дизрегуляторные функции при хондрогенезе, аутофагии хондроцитов, апоптозе, старении, внутриклеточной передаче сигналов и воспаления. Данные по хрящам, клеткам или плазме человека показаны слева. дополнительные данные от моделей мышей с правой стороны.
Fig. 2. Examples of the roles of microRNAs in osteoarthritis. A number of microRNAs have been shown to be dysregulated in osteoarthritic cartilage and to have functions in chondrogenesis, chondrocyte autophagy, apoptosis, senescence, intracellular signalling and inflammation. Data from human cartilage, cells or plasma is shown on the left hand side with complementary data from mouse models on the right hand side.