 Цель исследования
Цель исследования
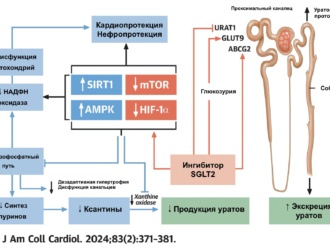
Изучить эффективность и безопасность применения пеглотиказы в комбинации с метотрексатом у пациентов с неконтролируемой подагрой в экспериментальном открытом клиническом исследовании (NCT03635957) в преддверии рандомизированного контролируемого исследования.
Методы
Проведено многоцентровое открытое исследование эффективности и безопасности применения пеглотиказы с одновременным применением метотрексата у пациентов с неконтролируемой подагрой.
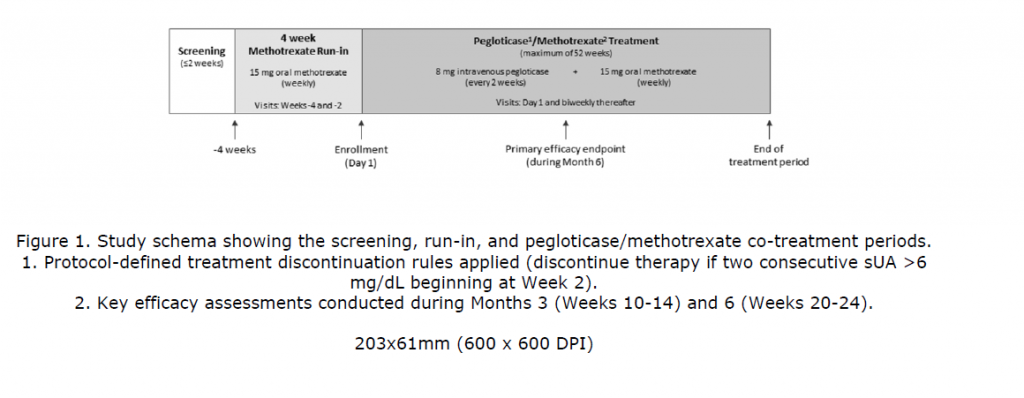
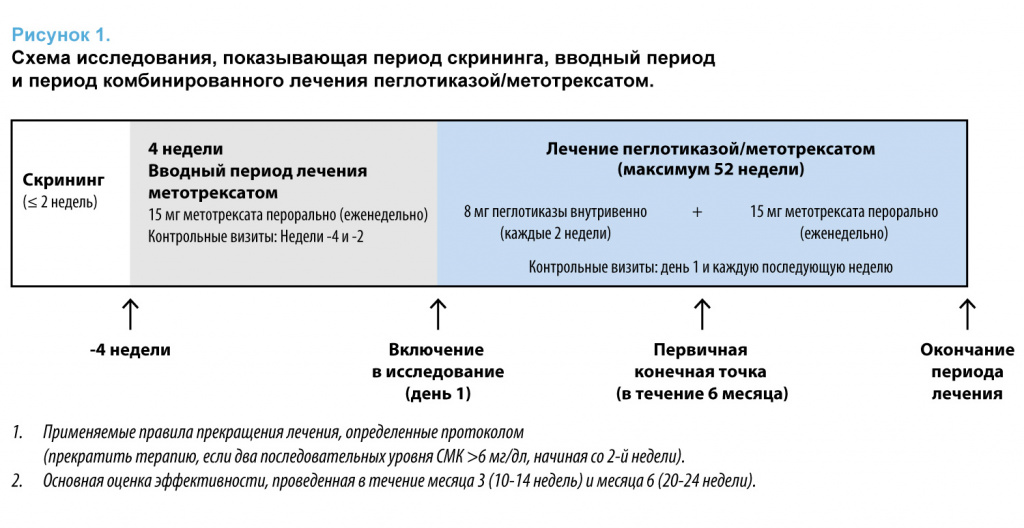
Пациенты принимали метотрексат (15 мг/нед) и фолиевую кислоту (1 мг/сут) перорально за 4 недели до начала и на протяжении всего лечения пеглотиказой.
Первичным результатом исследования была доля пациентов, ответивших на лечение, определяемая как СМК <6 мг/дл в течение ≥80% времени в течение 6-го месяца (20, 22 и 24 недели).
Все анализы проводились на основании модифицированной популяции, включающей в себя всех пациентов, первоначально отобранных для исследования, определяемой как пациенты, получившие более одной инфузии пеглотиказы.
Результаты
Было обследовано семнадцать пациентов, и 14 из них были включены в исследование (все мужского пола, средний возраст: 49,3 ± 8,7 года).
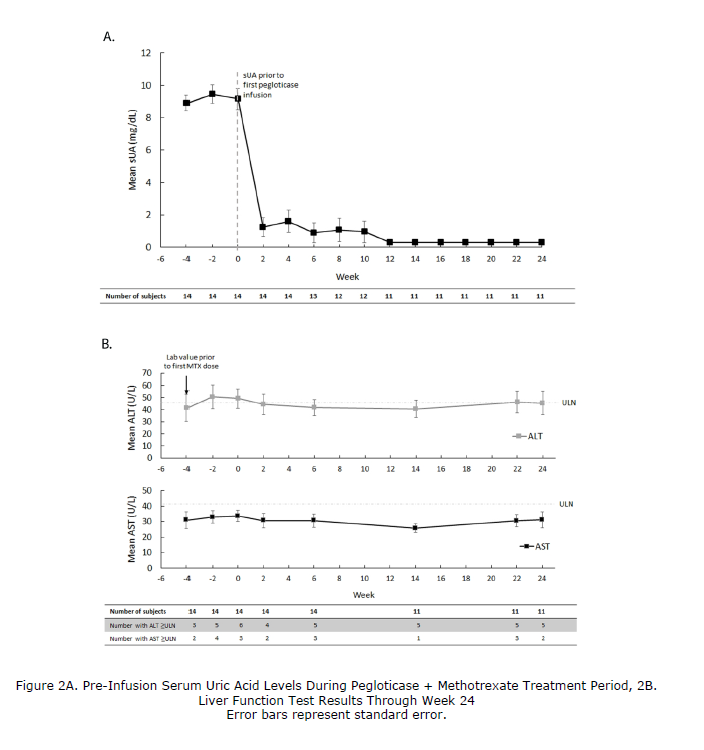
На день 1 исследования среднее значение СМК составило 9,2 ± 2,5 мг/дл, и у 12 из 14 пациентов наблюдались заметные тофусы.
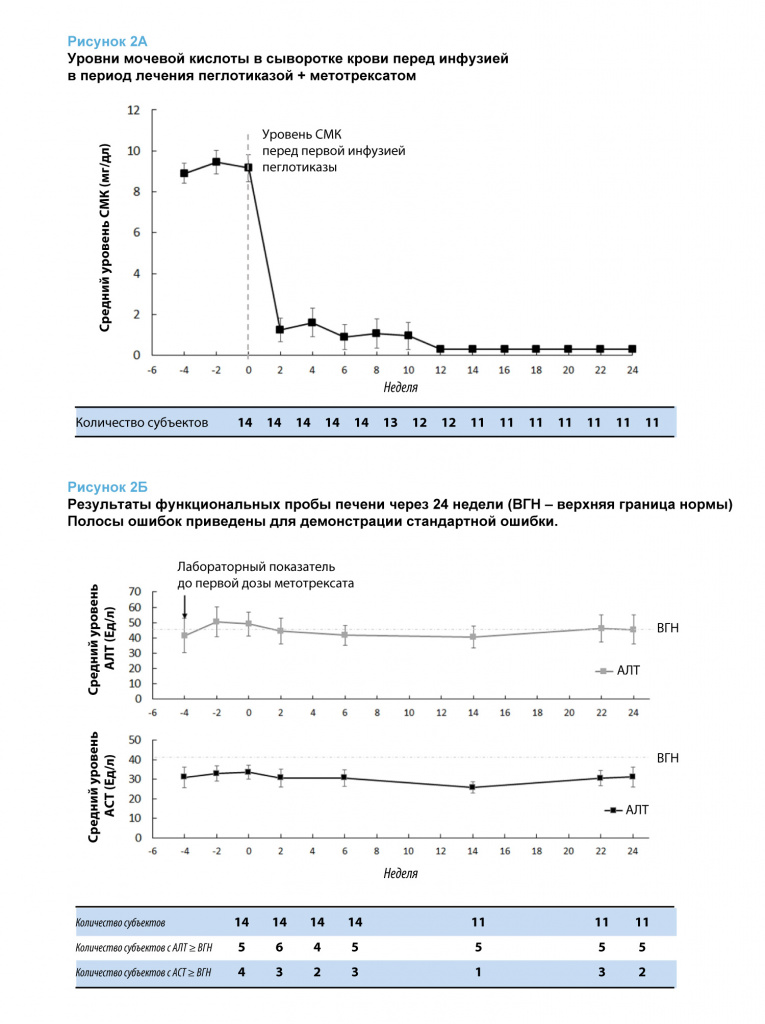
Через 6 месяцев 11 из 14 участников исследования (78,6%, 95% ДИ 49,2-95,3%) соответствовали критериям ответа на терапию, причем 3 пациента прекратили лечение по причине соответствия определенным протоколом правилам прекращения лечения (значения СМК перед инфузией превышали 6 мг/дл при 2 последовательных плановых визитах).
Все пациенты хорошо переносили метотрексат.
Никаких новых проблем в области безопасности выявлено не было.
Заключение
В этом исследовании доля пациентов, сохранявших терапевтический ответ в течение 6 месяцев при одновременном лечении метотрексатом и пеглотиказой, была выше по сравнению с ранее сообщенными 42% при использовании только пеглотиказы.
Эти результаты подтверждают необходимость рандомизированного исследования применения метотрексата или плацебо с пеглотиказой для подтверждения результатов открытого исследования.
John K Botson, John R P Tesser, Ralph Bennett, Howard M Kenney, Paul M Peloso, Katie Obermeyer, Brian LaMoreaux, Michael E Weinblatt, Jeff Peterson
J Rheumatol. 2020 Sep 15; jrheum
PMID: 32934137
DOI: 10.3899/jrheum.200460
Pegloticase in combination with methotrexate in patients with uncontrolled gout: A multicenter, open-label study (MIRROR)
Objective
To examine the efficacy and safety of pegloticase in combination with methotrexate in patients with uncontrolled gout in an exploratory, open-label clinical trial (NCT03635957) prior to a randomized, controlled trial.
Methods
A multicenter, open-label, efficacy and safety study of pegloticase with methotrexate cotreatment was conducted in patients with uncontrolled gout. Patients were administered oral methotrexate (15 mg/week) and folic acid (1 mg/day) 4 weeks prior to and throughout pegloticase treatment. The primary study outcome was the proportion of responders, defined as sUA <6 mg/dL for ≥80% of the time during month 6 (weeks 20, 22, and 24). All analyses were performed on a modified intent-to-treat population, defined as patients who received ≥1 pegloticase infusion.
Results
Seventeen patients were screened and 14 patients (all men, average age: 49.3 ± 8.7 years) were enrolled. On Day 1, mean sUA was 9.2 ± 2.5 mg/dL and 12 of the 14 patients had visible tophi. At the 6 month timepoint, 11/14 (78.6%, 95%CI 49.2-95.3%) met the responder definition, with 3 patients discontinuing after meeting protocol-defined treatment discontinuation rules (pre-infusion sUA values greater than 6 mg/dL at 2 consecutive scheduled visits). All patients tolerated methotrexate. No new safety concerns were identified.
Conclusion
In this study, an increased proportion of patients maintained therapeutic response at 6 months when treated concomitantly with methotrexate and pegloticase when compared to the previously reported 42% using pegloticase alone. These results support the need for a randomized study of methotrexate or placebo with pegloticase to validate these open label findings.