Aernoud T.L. Fiolet, MD1,2; Stefan M. Nidorf, MD, MBBS, FRACP3; Arend Mosterd, MD, PhD, FESC2,4; and Jan H. Cornel, MD, PhD, FESC5
Резюме
Цель: Ведение пациентов со стабильной ишемической болезнью сердца заключается в контроле параметров гемостаза и коррекции липидного обмена. На настоящий момент терапевтических средств, направленных на предотвращение эрозии и разрыва атеросклеротической бляшки, не имеется. Считается, что воспаление, индуцированное кристаллами холестерина и приводящее к дестабилизации атеросклеротической бляшки, является важным фактором нестабильности бляшки и возможно может поддаваться контролю противовоспалительными препаратами. Колхицин, как противовоспалительный препарат, обладает потенциалом к действию как на прямые, так и на косвенные механизмы воспаления, характерные для атеросклеротической бляшки.
Методика: Был проведен поиск литературы в базах MEDLINE (PubMed), EMBASE и Кокрановском центральном регистре контролируемых исследований, а также в регистрах клинических исследований с целью обнаружения завершенных и текущих клинических исследований по применению колхицина при стабильной ишемической болезни сердца.
Полученные данные: Результаты доклинических исследований по применению колхицина при стабильной ишемической болезни сердца показали наличие защитного действия в отношении суррогатных точек, таких как площадь поражения миокарда при инфаркте и рестеноз после ангиопластики. В ретроспективных когортных исследованиях с участием пациентов с подагрой была показана более низкая частота комбинированных сердечно-сосудистых точек у пациентов, получавших колхицин. На сегодняшний день доказательства возможного защитного эффекта колхицина при стабильной ишемической болезни сердца получены в одном проспективном рандомизированном клиническом исследовании. Мета-анализ исследований по применению колхицина при различных сердечно-сосудистых заболеваниях выявил снижение частоты инфаркта миокарда с различным уровнем доказательности. В настоящее время проводится набор участников в 5 крупных клинических исследований, в которых будут задействованы > 10 000 пациентов, и все они сосредоточены на основных сердечно-сосудистых исходах.
Выводы: Количество и качество объективных данных относительно эффективности колхицина для вторичной профилактики при стабильной и острой ишемической болезни сердца значительно увеличится в ближайшие годы, что обеспечит менее предвзятую и более точную оценку данного воздействия. Если будет показано, что противовоспалительные свойства колхицина способствуют повышению сердечно-сосудистой выживаемости без развития нежелательных явлений, то это относительно безопасное, недорогое и хорошо изученное лекарственное средство может стать третьим столпом (наряду с контролем уровня липидов и терапией антиагрегантами) в медикаментозной терапии стабильной ишемической болезни сердца.
Введение
Атеросклероз является медленно прогрессирующим заболеванием. Ишемическая болезнь сердца ответственна за >15% от общего числа смертей, входя в тройку самых важных неинфекционных заболеваний почти в каждой развитой стране [1-3]. Качество терапии атеросклероза значительно повысилось за последние 50 лет. Контроль образа жизни, дислипидемии и тромбоза позволил снизить связанные с ними показатели смертности на 25%-50% [1,4,5]. Однако даже при использовании данных терапевтических стратегий пациент со стабильной ишемической болезнью сердца в течение 5 лет имеет как минимум 15%-ный риск смерти от сердечно-сосудистых причин или развития любого значительного нежелательного сердечно-
сосудистого события [6-10]. Этот остаточный риск отражает биологический механизм развития атеротромбоза, который не поддается достаточному контролю липидснижающей и антитромботической терапией, и в основе которого лежит воспаление, управляющее развитием атеросклеротического процесса [11]. В недавно проведенных исследованиях, посвященных способности инновационных противовоспалительных препаратов влиять на этот механизм, были продемонстрированы разные эффекты.
Однако, и колхицин, применяемый десятилетиями, также продемонстрировал многообещающие результаты при стабильной ишемической болезни сердца. Колхицин недорогой препарат, доступный по всему миру, с доказанной безопасностью и эффективностью в лечении для ряда воспалительных заболеваний. Цель настоящей работы — обзор механизма действия колхицина при стабильной ишемической болезни сердца и резюме клинических данных относительно его эффективности и безопасности.
Материалы и методы
Для обобщения имеющегося массива данных была использована схема оценочного обзора с целью включения ряда исследований и сообщений в описательной форме. Для осуществления этой цели были отобраны литературные источники по результатам поиска в библиографических базах данных MEDLINE (PubMed), EMBASE и Кокрановском центральном регистре контролируемых исследований с использованием в качестве терминов поиска «колхицин» + «сердечно-сосудистые заболевания» или «колхицин» + «ишемическая болезнь сердца» и синонимов. Также использованы сходные поисковые термины при поиске в базе данных клинических исследований Национальной библиотеки медицины США (http://www.clinicaltrials.gov) и Австралийского и Новозеландского регистра клинических исследований (www.anzctr.org.au). Перекрестные ссылки проверялись для всех статей. Никаких языковых или издательских ограничений не применялось. Несмотря на то, что использовались поисковые термины широкого спектра, основное внимание уделялось исследованиям по применению колхицина на моделях атеросклероза или клиническим исследованиям при стабильной ишемической болезни сердца.
Воспаление при атеросклерозе, вызванное кристаллами холестерина
Множество провоцирующих факторов (например, гипертензия, дислипидемия, курение, метаболический синдром) приводит к дисфункции эндотелия сосудов и отложению частиц ЛПНП в интиме сосудов, с формированием в артериальной стенке асимметричных атеросклеротических бляшек, покрытых фиброзными покрышками [12,13].
Отложение нагруженных липидами макрофагов внутри артериальной стенки сопровождается развитием воспалительной реакцией на свободные кристаллы холестерина в интерстициальном пространстве. Холестерин может образовывать большие кристаллические структуры внутри бляшки, приводя к увеличению её объема; кристаллы, которые мигрируют на поверхность бляшки, могут перфорировать покрышку бляшки. Эмболизация кристаллами холестерина может вызвать дистальную ишемию и воспаление тканей [14,15].
Кроме того, кристаллы холестерина могут вызывать прямую воспалительную реакцию, реализующуюся за счет действия интерлейкинов, системы комплемента и нейтрофилов. Макрофаги реагируют на кристаллы активацией содержащего домены NACHT, LRR и PYD белка 3 (NLRP3) — инфламмасомы, отвечающей за высвобождение интерлейкина-1 бета, по аналогии с другими кристалл-индуцированными патологическими состояниями [16-20]. Также могут отмечаться косвенные провоспалительные эффекты. По мере формирования кристаллы холестерина обычно покрываются белками, включая белки системы комплемента и аполипопротеины, что делает их инертными во внеклеточном пространстве [21]. Непокрытые кристаллы обладают способностью к расщеплению факторов комплемента, в том числе C3 и C5. Это действие может усилить местный воспалительный ответ путем стимуляции экспрессии е-селектина на поверхности эндотелиальных клеток, что способствует перемещению циркулирующих нейтрофилов в интерстициальное пространство, окружающее центральную зону бляшки, и прямой активации нейтрофилов. При невыраженном воспалительном стимуле развивается хроническое воспаление, что приводит к прогрессирующему утолщению, кальцификации и деформации стенки сосуда. При более выраженном атеросклеротическом процессе воспалительная реакция может усилиться и оказаться достаточной для эрозии или полного разрушения бляшки, что приводит к атеротромбозу [12,13,22].
Таким образом, NLRP3-опосредованный провоспалительный ответ на кристаллы холестерина в бляшке имеет сходство с кристалл-индуцированным воспалением, вызванным отложением кристаллов урата натрия [23]. Гиперурикемия, приводящая к образованию кристаллов урата натрия, приводит к развитию подагры. При данном состоянии на протяжении столетий эффективно применяется колхицин [24,25].
Сложность и комплексность воспалительного процесса при атеросклерозе более изучена на данный момент, но только частично может быть объяснена взаимодействием системы комплемента, интерлейкинов и нейтрофилов. Известно, что ингибирование одного или более из данных воспалительных элементов может привести к клиническому улучшению у отдельных пациентов [26]. Представляется разумным предположение, что широкий противовоспалительный профиль действия колхицина может затрагивать различные механизмы развития воспаления, а не действовать только на один их них.
Данные по применению колхицина при стабильной ишемической болезни сердца
Ретроспективные исследования: оценка сердечно-сосудистых исходов у пациентов с подагрой.
В исследованиях, проведенных на животных, начавшихся еще в 1970-х годах, была показана способность колхицина ингибировать развитие атеросклероза независимо от терапии статинами и снижать риск рестеноза стента, но клинические данные появились в течение последнего десятилетия [27-29].
В двух ретроспективных наблюдательных исследованиях изучалось применение колхицина у пациентов с подагрой (Таблица I). В первом проводилась общая оценка взаимосвязи применения колхицина и частоты развития инфаркта миокарда [30].
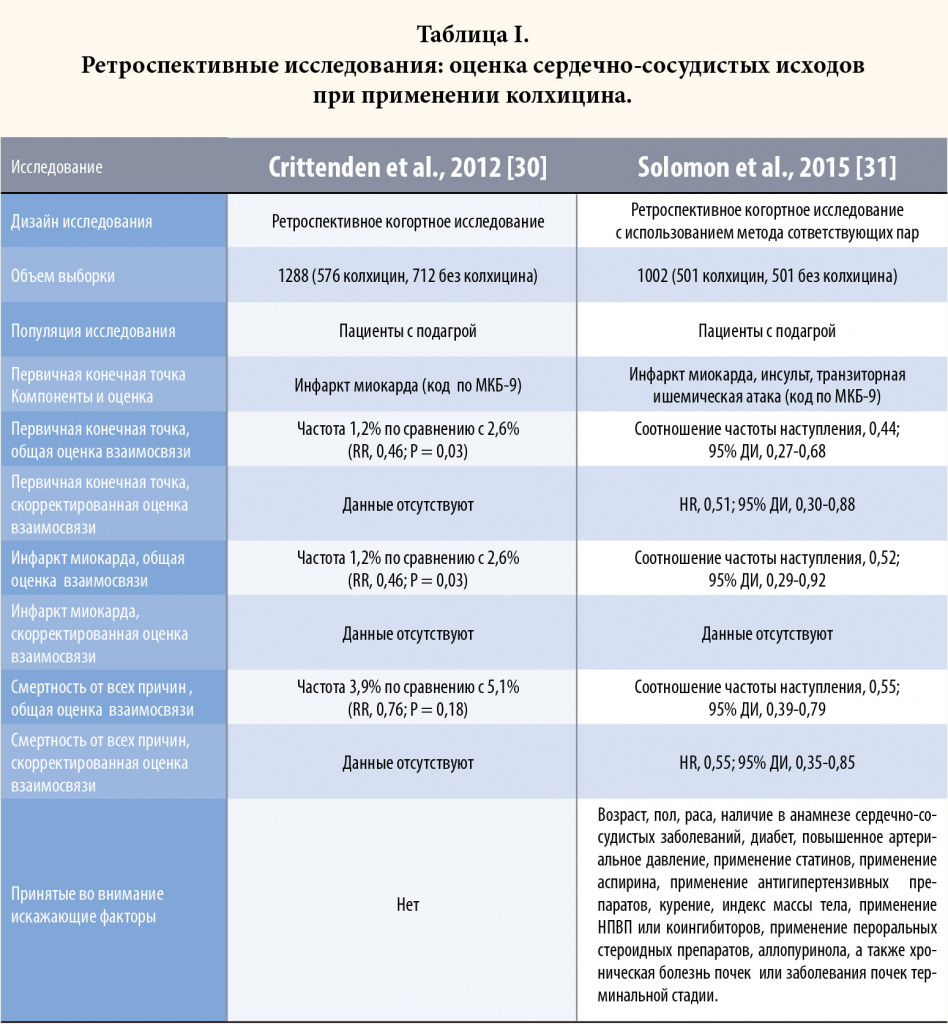
В когорте пациентов с подагрой 576 пациентов получали колхицин, 712 не получали. Частота инфаркта миокарда была ниже в когорте пациентов, получавших колхицин, по сравнению с не получавшими (1,2% против 2,6%; Р = 0,03). Однако остается неясным, предшествовало ли наступление события проводимому лечению, также в анализе не были учтены разница в характере течения заболевания или внешние факторы.
Второе исследование было проведено с участием 501 пациента с подагрой, которым был назначен колхицин, и с участием такого же количества соответствующих пациентов без применения колхицина [31]. Частота инфаркта миокарда, инсульта или транзиторной ишемической атаки на 1000 человеко-лет составила 35,6 для пациентов, принимавших колхицин, и 81,8 – для участников, не принимавших колхицин, что соответствует снижению риска на 49% (отношение рисков [HR], 0,51; 95% ДИ, 0,30-0,88) с учетом корректировки по искажающим факторам. Для показателя смертности от всех причин наблюдалось снижение на 73% (скорректированное HR, 0,27; 95% ДИ, 0,17-0,43). В исследованиях данного дизайна остается высоким риск остаточных искажений за счет различий в показаниях к применению, однако это не уменьшает их важности как исследований для поиска гипотезы.
Проспективные исследования: колхицин у пациентов со стабильной ишемической болезнью сердца.
Ряд исследований показал, что низкие дозы колхицина могут достоверно снижать уровни воспалительных маркеров, включая высокочувствительный С-реактивный белок
(hs-СРБ) и интерлейкин-6, у пациентов с сердечной недостаточностью и у пациентов, подвергшихся абляции при фибрилляции предсердий; однако оценка влияния колхицина на биохимические параметры у пациентов со стабильной ишемической болезнью сердца была проведена только в одном рандомизированном исследовании [32-34].
У 64 пациентов со стабильной ишемической болезнью сердца с повышенным уровень hs-CРБ, несмотря на терапию статинами в высокой дозе, применение колхицина в дозировке 0,5 мг дважды в сутки достоверно и быстро снижало уровень hs-CРБ в течение 4 недель. Данное наблюдение позволило предположить, что колхицин может оказывать противовоспалительное действие, выходящее за рамки действия статинов и антитромбоцитарной терапии. Эти находки также легли в основу первого исследования LoDoCo (низкие дозы колхицина), в котором изучали влияние применения колхицина у пациентов со стабильной ишемической болезнью сердца, получающих оптимальную терапию и которых набирали в исследование без учета исходного уровня hs-СРБ [35].
В исследовании LoDoCo использовали дизайн проспективного, рандомизированного, слепого исследования с конечными точками, в котором пациенты были распределены в группы применения либо колхицина 0,5 мг один раз в≈день, либо регулярного клинического наблюдения [35]. По окончании периода последующего наблюдения, медиана 3 года, наблюдалась значительная разница в пользу применения колхицином по частоте достижения первичных конечных точек (HR, 0,33; 95% ДИ, 0,18-0,59). Первичная конечная очка включала смерть от сердечно-сосудистых причин, некардиоэмболический инсульт, острый коронарный синдром и внебольничную остановку сердца. В основном это снижение было обусловлено снижением частоты острого коронарного синдрома (72%), где более половины составляли случаи нестабильной стенокардии, независимо от проведения реваскуляризации. Риск систематической ошибки наблюдателя должен быть сведен к минимуму с помощью слепой оценки конечной точки, хотя систематическая ошибка остаточной информации все еще могла играть определенную роль при принятии решений о выборе терапии. Однако это весьма прагматичное исследование предоставило первые клинические данные об эффективности применения колхицина для вторичной профилактики при стабильной ишемической болезни сердца. Оно заложило основу для обоснования и разработки дизайна более крупных, более достоверных плацебо-контролируемых исследований фазы III.
Проспективные исследования: колхицин у пациентов, перенесших коронарную ангиопластику и стентирование.
В двух проспективных рандомизированных плацебо-контролируемых исследованиях изучалось влияние колхицина на рестеноз после коронарной ангиопластики.
В первое были включены 197 пациентов, перенесших баллонную ангиопластику, где было показано, что применение колхицина 0,6 мг два раза в сутки в течение 6 месяцев не способствовало снижению частоты рестеноза [36]. Во втором исследовании приняли участие 196 пациентов с сахарным диабетом, которым проводили лечение с установкой металлического стента без покрытия; в данном исследовании было показано, что применение колхицина 0,5 мг в течение 6 месяцев два раза в сутки приводило к снижению в 2 раза частоты ин-стент рестеноза по данным ангиографии (16% по сравнению с 33%; P 0,007). В совокупности полученные результаты могут свидетельствовать о том, что колхицин не влияет на ранний рестеноз, связанный с эластической тягой, после баллонной ангиопластики, но может предотвращать гиперплазию неоинтимы, приводящую к раннему ин-стент рестенозу, как было показано в моделях на животных [38].
Текущие и планируемые проспективные исследования: колхицин при ишемической болезни сердца.
В настоящее время пять клинических исследований III фазы, в которых изучается применение низких доз колхицина у пациентов с ишемической болезнью сердца, находятся в стадии разработки или набора участников (Таблица II).
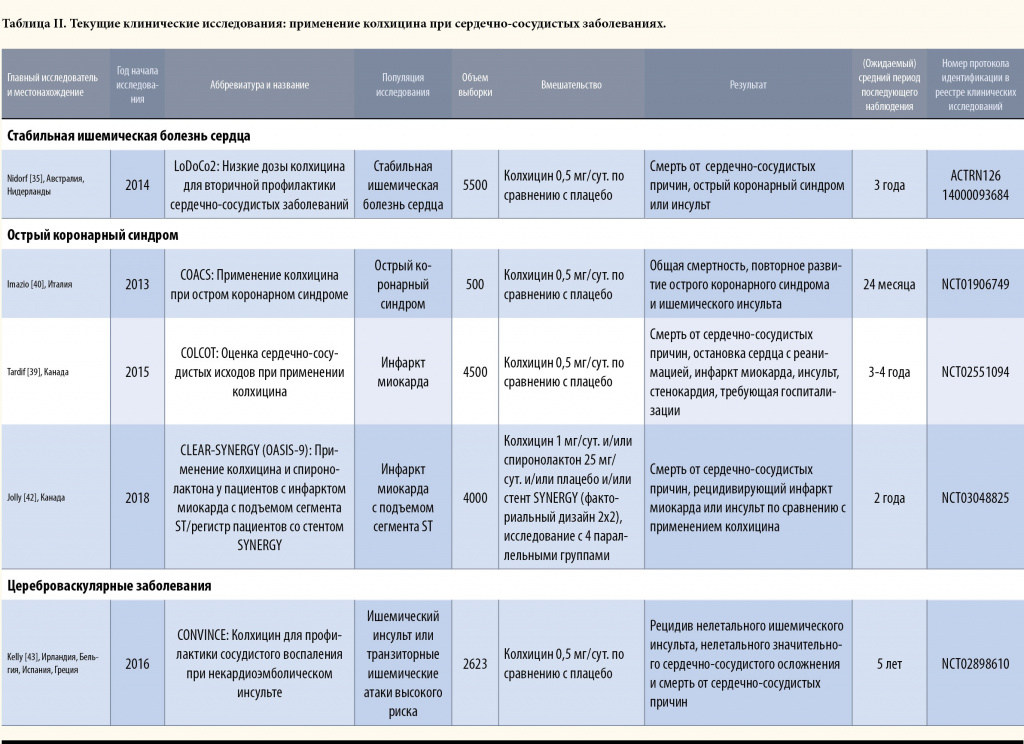
В два из трех уже начатых исследований производится набор пациентов, недавно перенесших острый коронарный синдром: COLCOT (Colchicine Cardiovascular Outcomes Trial — Сердечно-сосудистые исходы у пациентов, получающих колхицин) в Канаде и COACS (Colchicine for Acute Coronary Syndromes — Применение колхицина при остром коронарном синдроме) в Италии [39,40]. В исследовании LoDoCo2 в Австралии и Нидерландах изучают применение колхицина в дозировке 0,5 мг у пациентов со стабильным течением ишемической болезни сердца в течение 6 месяцев до включения в исследование [41]. Набор участников в него проводят без привязки к базовому уровню воспаления. Исследование включает 30-дневною открытую вводную фазу для колхицина. Первичная конечная точка включает такие события, как смерть от сердечно-сосудистых причин, инфаркт миокарда, ишемический инсульт и нестабильная стенокардия, потребовавшая проведения реваскуляризации. Когорта участников отражает гетерогенную группу пациентов с ишемической болезнью сердца в возрасте 45-82 лет, получающих оптимальную терапию. Есть надежда, что по всем исследованиям отчеты будут предоставлены в 2020 году, в зависимости от накопления достаточного количества событий.
Два исследования фазы III по применению колхицина у пациентов с атеросклерозом находятся на завершающей стадии планирования и, вероятно, в этом году начнется набор пациентов. В исследовании CLEAR-SYNERGY (OASIS-9; Colchicine and Spironolactone in Patients With STEMI/SYNERGY Stent Registry — Применение колхицина и спиронолактона у пациентов с инфарктом миокарда с подъемом сегмента ST/регистр пациентов со стентом SYNERGY) был использован факториальный дизайн 2×2 с целью изучения влияния колхицина 1 мг/сут. по сравнению с применением спиронолактона или плацебо у 4000 пациентов, недавно перенесших инфаркт миокарда с подъемом сегмента ST [42]. В исследовании CONVINCE (Colchicine for Prevention of Vascular Inflammation in Non-cardio Embolic Stroke — Колхицин для профилактики сосудистого воспаления при некардиоэмболическом инсульте) исследуется влияние применения колхицина в дозе 0,5 мг в сутки на сердечно-сосудистые исходы у ~2500 пациентов с предшествующей симптоматической цереброваскулярной болезнью [43]. Первичная конечная точка в обоих исследованиях включает только смерть от сердечно-сосудистых причин, инфаркт миокарда и инсульт, и результаты по данным исследованиям, вероятно, будут представлены в 2022 году.
Мета-анализ: применение колхицина и сердечно-сосудистые исходы
В двух мета-анализах изучалось влияние колхицина на сердечно-сосудистую систему на основе результатов ряда проспективных клинических исследований (Таблица III). В мета-анализе, проведенном Кокрановской группой, были изучены сердечно-сосудистые исходы и применение колхицина у 4992 пациентов в 39 рандомизированных контролируемых исследованиях с более широким кругом пациентов с сердечно-сосудистыми заболеваниями и без них [44]. В целом было установлено, что колхицин не оказывает влияния на смертность от всех причин (относительный риск 0,94; 95% ДИ, 0,82-1,09), но доказательная база данных исследований обладает качеством от низкого до умеренного.

Риск инфаркта миокарда снижался,но были представлены данные с ограниченной доказательностью с широкими ДИ (относительный риск 0,20; 95% ДИ, 0,07-0,57; 2 исследования). Не было выявлено влияния колхицина на общие нежелательные явления, хотя наблюдалось повышение желудочно-кишечной непереносимости. В мета-анализе, сфокусированном только на 5 исследованиях, в которые был включен 1301 пациент с сердечно-сосудистыми заболеваниями (ишемическая болезнь сердца, острый коронарный синдром или инсульт, период после ангиопластики или застойная сердечная недостаточность), на объе-
диненных данных было показано снижение частоты комбинированных сердечно-сосудистых исходов на ~60% (относительный риск, 0,44; 95% ДИ, 0,28-0,69) у пациентов, принимавших колхицин [45].
Безопасность и длительное применение колхицина при стабильной ишемической болезни сердца
Непрерывное применение колхицина практикуется десятилетиями в качестве вторичной меры профилактики ряда воспалительных состояний, из которых наиболее значимыми являются подагра и семейная средиземноморская лихорадка, в результате чего накоплено много информации относительно переносимости и токсичности препарата [46-48]. От 5 до 10 процентов пациентов испытывают ранние побочные эффекты легкой степени со стороны желудочно-кишечного тракта в начале лечения при дозе 0,5 мг в день, которые обычно самопроизвольно разрешаются. Общая частота развития поздней непереносимости колхицина является низкой и сходной с таковой как при терапии низкими дозами аспирина и статинами [49,50].
Оценка, проведенная Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США, показала, что колхицин при применении в терапевтических дозах, скорректированных с учетом функции печени и почек, обладает хорошей переносимостью. Даже при длительном применении побочные явления, за исключением нарушений со стороны желудочно-кишечного тракта, наблюдаются у <15% пациентов, и чаще всего они возникают при неправильном дозировании у лиц с почечной или печеночной недостаточностью, при взаимодействии с другими препаратами или при передозировке. Тяжелые гематологические нарушения (например, лейкопения, агранулоцитоз, панцитопения) встречаются редко и, по-видимому, связаны с высокими суточными дозами у пациентов с почечной недостаточностью терминальной стадии [51-54].
Препараты, ингибирующее P-гликопротеин, или систему цитохрома P450 3A4, или метаболизируемые с участием данного фермента, могут способствовать повышению уровня колхицина и как следствие развитию токсического эффекта, особенно в случае общего снижения уровня метаболизма и выведения, например при печеночной или почечной недостаточности [54-56]. Кларитромицин представляется наиболее значимым препаратом в этом отношении [57-59].
Из-за методологических трудностей данные, касающиеся взаимодействия при длительном применении колхицина и статинов и возникновения миопатии, ограниченны [60,61]. Профиль взаимодействия основан на фармакокинетических параметрах и отдельных сообщениях о клинических случаях [62,63]. Существует двунаправленное взаимодействие между колхицином и статинами, приводящее к повышению концентрации обоих соединений и к возникновению связанных побочных эффектов [60,62,64].
У пациентов, принимающих статины и колхицин, отмечается повышенный риск развития миопатии или миотоксичности, но данное явление наблюдается только у пациентов с легкой или тяжелой почечной недостаточностью [65,66]. Потенциал рисков и клинической значимости миопатии у пациентов, принимающих одновременно статины и колхицин, будет более ясен, когда будут доступны результаты текущих клинических исследований. На данный момент совместное применение низких доз колхицина и статинов считается целесообразным при условии мониторинга признаков мышечной токсичности [64].
Противогрибковые препараты группы имидазола, ингибиторы протеазы и циклоспорин являются одновременно как ингибиторами цитохрома P450 3A4, так и P-гликопротеина, и их применение может приводить к повышению концентрации колхицина. Это вид взаимодействия описан только для кетоконазола в небольшом количестве сообщений об отдельных случаях [46,62,67,68].
Выводы
Современные данные свидетельствуют о том, что медленно прогрессирующий характер атеросклероза лучше всего можно регулировать, обращаясь к 3 основным столпам болезни: контроль дислипидемии, гемостаза и воспалительной реакции. Воспаление, индуцированное кристаллами холестерина, представляет собой взаимодействие интерлейкинов, нейтрофилов и системы комплемента. Колхицин обладает способностью тормозить множество клеточных каскадов, и в ряде клинических исследований были продемонстрированы его защитные эффекты при стабильной ишемической болезни сердца. Кроме того, препарат представляется безопасным при длительном применении в случае различных сердечно-сосудистых заболеваний. Ожидается, что в предстоящие годы будет расширена доказательная база о его эффективности при стабильной и острой ишемической болезни сердца. Эта информация, безусловно, поможет определить, будет ли этот хорошо известный недорогой препарат иметь дополнительную ценность в отношении контроля воспаления при ишемической болезни сердца, отличительной биологической особенности атеросклероза.
Вклад авторов
Д-р Fiolet внес существенный вклад в концепцию и дизайн исследования, сбор, изучение и интерпретацию данных; а также в дизайн статьи. Д-ра Nidorf и Mosterd внесли существенный вклад в дизайн исследования, интерпретацию данных и проект статьи. Д-р Cornel внес существенный вклад в интерпретацию данных, проект статьи и редактуру рукописи с критической точки зрения на интеллектуальное содержание. Все авторы прочитали и одобрили окончательный вариант рукописи.
Концепция этой рукописи была выполнена без финансовой поддержки от какого-либо финансирующего учреждения или гранта. Авторы задействованы в научных исследованиях при поддержке грантов от ZonMw (Нидерландской организации медицинских исследований и разработок), Нидерландского Фонда Сердца, Австралийского национального совета по здравоохранению и медицинским исследованиям и generic pharma. JHC принимает участие в комитете по наблюдению за результатами исследования по влиянию применения канакинумаба на противовоспалительные исходы при тромбозе (CANTOS).
Конфликт интересов
Авторы заявляют, что у них отсутствуют конфликты интересов в отношении содержания этой статьи ◼
(Clin Ther. 2019;41: 30-40)
© 2018 Опубликовано Elsevier Inc.
Ключевые слова: противовоспалительные препараты, клинические исследования, колхицин, ишемическая болезнь сердца, повторное открытие препарата, инфаркт миокарда.
Fiolet ATL, Nidorf SM, Mosterd A, Cornel JH.Colchicine in Stable Coronary Artery Disease.
Clin Ther. 2019 Jan;41(1):30-40. doi: 10.1016/j.clinthera.2018.09.011. Epub 2018 Nov 2
Перевод и публикация выполнена с разрешения Elsevier.
1 Department of Cardiology, University Medical Centre Utrecht, Utrecht, the Netherlands; 2 Dutch Network for Cardiovascular Research (WCN), Utrecht, the Netherlands; 3 Heart Care Western Australia, Perth, Western Australia, Australia; 4 Department of Cardiology, Meander Medisch Centrum, Amersfoort, the Netherlands; and 5 Department of Cardiology, Northwest Clinics, Alkmaar, the Netherlands